V Laboratóriu špeciálnych metód máme možnosť analyzovať v krvi aj v moči všetky hormóny a prekurzory kôry i drene nadobličiek, a tak môžeme potvrdiť, alebo vyvrátiť suspektnú diagnózu. Stanovujeme pregnenolón, progesterón, 17-OH-progesterón, androstendión, DHES, kortizol, aldosterón, testosterón, dihydrotestosterón, estradiol, adrenalín, noradrenalín, dopamín, metanefrín, normetanefrín a kyselinu homovanilovú. Analyzujeme aj ACTH a renín. Máme vlastné skúsenosti a v spolupráci s Národným endokrinologickým a diabetologickým ústavom (NEDÚ) a viacerými endokrinológmi máme „vyliečených“ viac než 150 pacientov s ochorením nadobličiek.
Úvod do problematiky
Artériová hypertenzia (AH) je ochorenie a závažný rizikový faktor, ktorý sa významne podieľa na kardiovaskulárnej a cerebrálnej morbidite aj mortalite. Takmer 15 % AH spôsobuje endokrinná hypertenzia a môže byť spôsobená viacerými endokrinnými ochoreniami, najčastejšie však ochorením kôry a drene nadobličiek a ochorením hypofýzy. Nové poznatky v endokrinológii poukazujú na skutočnosť, že v spektre artériovej hypertenzie má sekundárna, hormonálne podmienená hypertenzia spôsobená hypersekréciou nadobličkových hormónov väčšie zastúpenie, než sa predpokladalo. Presnejšiu diagnostiku umožnilo práve meranie hormónov kôry a drene nadobličiek. Endokrinné ochorenie spôsobuje ťažkú hypertenziu s vážnymi orgánovými komplikáciami, avšak na strane druhej je liečiteľná. Je veľmi dôležité, aby internisti, kardiológovia alebo endokrinológovia včas rozpoznali endokrinné ochorenie ako príčinu hypertenzie a správne toto ochorenie liečili. Na našom oddelení sme diagnostikovali feochromocytóm u viacerých pacientov, ktorých poslal psychiater a tiež rádiológ, ktorý nás pri CT vyšetrení žlčníka upozornil na možný paraganglióm – ten sme následne potvrdili. Pri nízkej prevalencii hormonálne aktívnych nádorov nadobličiek nemajú ani erudovaní lekári dostatok skúseností s ich diagnostikou. V bežnej rutinnej praxi sa na tieto choroby zabúda. „Typický“ klinický obraz, ako je opísaný v učebniciach, je zriedkavý. Symptomatológia sa neraz ničím nelíši od bežnej esenciálnej hypertenzie. Hoci diagnostika nádorov nadobličiek patrí do rúk endokrinológa, záchyt týchto vážnych ochorení závisí významne od erudície lekárov prvého kontaktu. (Podoba, Trejbalová, Štekláč, 2005) Úloha praktického lekára je teda nesmierne dôležitá – musí pacienta nasmerovať k endokrinológovi. Pre endokrinnú hypertenziu je charakteristické to, že okrem vysokého krvného tlaku v klinickom obraze dominujú aj príznaky základného endokrinného ochorenia. Nadoblička, ako komplexný endokrinný orgán zložený z dvoch fyziologicky a embryologicky rozličných častí – z kôry a drene, produkuje široké spektrum steroidných hormónov a neurotransmiterov, ktorých hlavnou funkciou je príprava organizmu na zvládnutie fyzickej a psychickej záťaže. Nadobličky (NO) vylučujú hormóny, ktoré regulujú krvný tlak a srdcovú frekvenciu, rovnako ako hormóny, ktoré riadia spôsob využívania bielkovín, tukov a sacharidov. Porucha v syntéze, sekrécii alebo v regulácii môže viesť k rozvoju dramatických objektívnych príznakov. Najvýznamnejšie sú hormonálne aktívne nádory nadobličiek: dreňový feochromocytóm a kôrové adenómy spôsobujúce primárny aldosteronizmus a hyperkortizolizmus. Klinické aspekty týchto zriedkavých ochorení sú však mimoriadne významné. Pri správnej diagnostike ide väčšinou o úplne vyliečiteľné stavy. Ak sa však ochorenie nerozpozná a správne nelieči, môže spôsobiť vážne komplikácie až smrť pacienta. Ako som už spomínal, najdôležitejšie miesto v diagnostike má špecialista – endokrinológ, rovnako dôležité miesto však patrí aj lekárovi prvého kontaktu. Jeho úlohou je vybrať z veľkého množstva hypertonikov na cielené endokrinologické vyšetrenie tých, u ktorých vzniká na základe klinického obrazu opodstatnené podozrenie na hormonálne podmienenú artériovú hypertenziu.
Anatómia nadobličiek
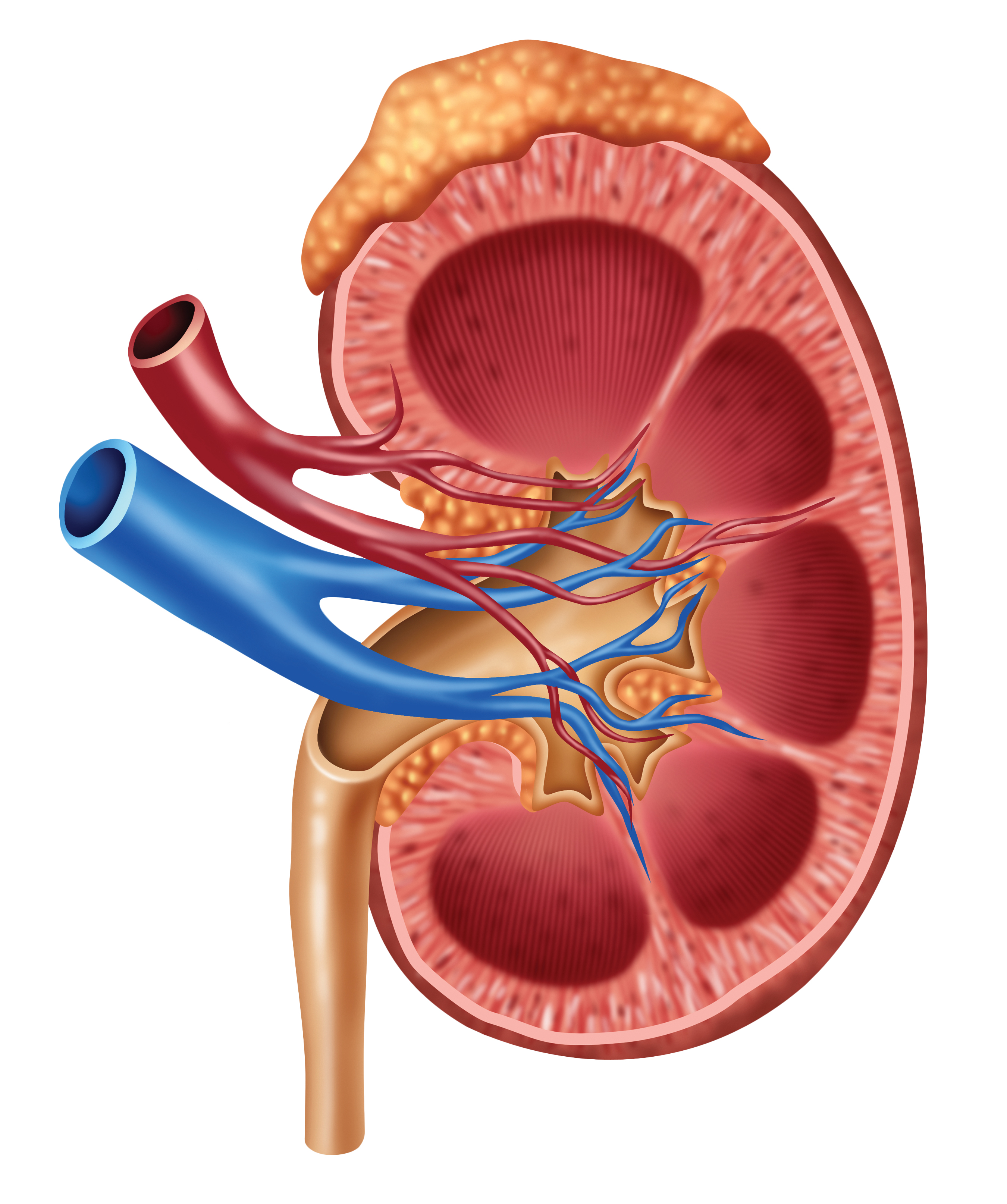
Nadobličky (Glandulae suprarenales) sú malé žltkasté orgány, ktoré sa nachádzajú na horných póloch obličiek v Gerota fascie (je to vrstva spojivového tkaniva, ktoré umožňuje zapuzdrenie obličiek a nadobličiek). Váha nadobličky sa zvyšuje vekom ku konečnej hmotnosti 4 – 5 g. Arteriálna krv na napájanie nadobličiek prichádza z a. coeliaca, mesenterica superior, phrenica inferior, renalis a aj z aorty. Tieto sa v NO rozvetvujú a vytvárajú kapilárne sínusoidy. Vysoká bazálna úroveň prietoku je v oboch častiach udržiavaná oxidom dusnatým. Odtok krvi zabezpečuje centrálna véna a krv tečie priamo do dolnej dutej žily (v. cava) na pravej a na ľavej strane do renálnej žily (v. renalis). Dreň nadobličky vzniká z primitívnych sympatikových buniek pochádzajúcich z neuroektodermu. Po pôrode tieto extraadrenálne chromafinné štruktúry obyčajne zanikajú, avšak v niektorých prípadoch z nich môže v neskoršom veku vzniknúť feochromocytóm. Z endokrinologického hľadiska sa nadobličky skladajú z dvoch odlišných endokrinných tkanív: kôra predstavuje 80 – 90 % objemu orgánu a produkuje kortikosteroidy, zatiaľ čo dreň tvorí katecholamíny. Hoci sú tieto dve časti v tesnom anatomickom spojení, fungujú a sú regulované nezávisle od seba.
Zloženie kôry NO:
zona glomerulosa – tvoria sa tu mineralokortikoidy (najdôležitejší je aldosterón), nachádza sa pod kapsulou a tvorí okolo 5 % objemu kôry,
zona fasciculata (okolo 70 % objemu), tvoria sa tu glukokortikoidy (prevažne kortizol),
zona reticularis (okolo 25 % objemu), vylučuje androgény (najmä dehydroepiandrosterón).
Steroidné hormóny kôry môžeme rozdeliť do 3 skupín:
21-C-kortikosteroidy – patria sem glukokortikoidy a mineralokortikoidy,
19-C-steroidy – patria sem prirodzené androgény (odvodené od androstánu),
18-C-steroidy – patria sem prirodzené estrogény (odvodené od estránu).
Posledné dve vrstvy tvoria funkčnú jednotku, lebo produkujú kortizol aj androgény. Skupiny hormónov podľa prevažujúceho účinku delíme na glukokortikoidy, mineralokortikoidy, estrogény a androgény.
Biosyntéza hormónov kôry a drene nadobličky (Obrázok č. 1)
Cholesterol je všeobecným prekurzorom všetkých steroidných hormónov vrátane adrenálnych steroidov. Väčšina cholesterolu používaná pri steroidogenéze sa získava degradáciou cirkulujúceho LDL cholesterolu. V lyzozómoch sa tento typ lipoproteínov viaže na špecifické receptory na membráne kortikálnych buniek, potom vstupuje do bunky mechanizmom endocytózy a degraduje sa uvoľnením voľného cholesterolu. Tá časť cholesterolu, ktorá sa nepoužije na biosyntézu steroidov, sa esterifikuje a ukladá v cytoplazmatických vakuolách. Ak sa ukáže zvýšená potreba cholesterolu na steroidogenézu, tieto uložené estery sa hydrolyzujú pomocou cytoplazmatických enzýmov za vzniku voľného cholesterolu. Adrenokortikálne bunky však môžu produkovať cholesterol aj priamo de novo syntézou z acetátu. Limitujúcim krokom pri biosyntéze steroidov je intracelulárny transport cholesterolu z vnútrobunkových zásob na vnútornú membránu mitochondrií, kde dochádza k odbúraniu vedľajšieho reťazca cholesterolu pomocou systému skladajúceho sa z enzýmu CYP11A, adrenodoxínu a reduktázy. Na biosyntéze steroidných hormónov sa zúčastňujú dve skupiny enzýmov: enzýmy cytochrómu P450 a enzýmy dehydrogenázy s krátkym reťazcom. Tieto enzýmy sa nachádzajú jednak v hladkom endoplazmatickom retikule (ER) a jednak vo vnútornej mitochondriálnej membráne, čo sú dve štruktúry, medzi ktorými „premávajú“ jednotlivé steroidy počas biosyntézy. Z cholesterolu sa tvorí hydroxyláciou a následným odštiepením šesťuhlíkatého bočného reťazca pregnenolón, ktorý sa v mikrozómoch ER premieňa na progesterón, ktorý sa účinkom následných hydroxylácií mení na 17α-hydroxyprogesterón, 11-deoxykortizol a kortizol. Progesterón sa však v prvom stupni hydroxylácie môže meniť na 11-deoxykortikosterón a v ďalšom kroku sa hydroxyláciou mení na kortikosterón – východiskový produkt pre syntézu aldosterónu. Aldosterón sa tvorí v zona glomerulosa a hydroxyláciou sa mení na 18-hydroxykortikosterón a následnou dehydrogenáciou vzniká aldosterón. Nadobličkové androgény (v zona reticularis) z progesterónu alebo pregnenolónu sa menia 17-hydroxyaláciou a vzniká 17α-hydroxyprogesterón a 17α-hydroxypregnenolón – odštiepením bočného reťazca sa z C17 tvoria C19 steroidy dehydroepiandrosterón a androstendión. V malých množstvách sa tvorí testosterón, ktorý sa účinkom aromatáz mení na estradiol a androstendión sa mení na estrón a tieto sú v malých množstvách secernované do krvi (v menopauze alebo po ovariektómii je NO hlavným zdrojom estrogénov). Steroidné hormóny sa po syntéze neukladajú do zásoby v bunkách – vylučujú sa s niektorými svojimi prekurzormi do krvi. Hlavným mineralokortikoidom je aldosterón, hlavným glukokortikoidom je kortizol a hlavným androgénnym steroidom je dehydroepiandrosterón. Hormóny sú vylučované do krvi ako voľné hormóny, ktoré sa v plazme viažu na bielkovinové nosiče. Voľné a viazané frakcie hormónov sú v rovnováhe, biologicky aktívne sú voľné hormóny – cez receptory môžu vstupovať do tkanív. Kortizol sa viaže na proteíny v krvi, a to predovšetkým na kortizol viažuci globulín alebo transkortín. Viac ako 90 % kortizolu sa transportuje v krvi práve v tejto viazanej forme. Naopak, iba 50% aldosterónu sa viaže na proteín v krvi. Všetky adrenokortikálne steroidy sú degradované v pečeni a prevažne konjugované na glukuronidy a v menšom množstve na sulfáty. Asi 75 % z týchto degradačných produktov je vylučovaných močom a zvyšok sa vylučuje žlčou. (Kreze, 2004)

Aldosterón
Je hlavným mineralokortikoidom, ktorý sa normálne tvorí iba v zóne glomerulosa. Jeho biosyntéza prebieha rovnako ako v prípade kortizolu až na to, že v prvom kroku nedochádza k 17α-hydroxylácii, lebo CYP17 sa nenachádza v zona glomerulosa. Sekrécia jeho prekurzoru 18-hydroxykortikosterónu je paralelná so sekréciou aldosterónu. Aldosterón je najsilnejším mineralokortikoidom a ďalšie steroidy majú nižšiu mineralokortikoidovú účinnosť (11-deoxykortikosterón, 18-hydroxydeoxykortikosterón, kortikosterón a kortizol), podobne ako niektoré ich metabolity (napr. 19-nordeoxykortikosterón). V patologických situáciách (nadobličkový tumor alebo kongenitálna adrenálna hyperplázia) však môžu aj tieto látky významne prispievať k mineralokortikoidovej aktivite. Aldosterón predstavuje 90 % mineralokortikoidnej aktivity, nejakou aktivitou prispievajú aj deoxykortikosterón, kortikosterón a kortizol. Regulácia syntézy – a tým aj sekrécia aldosterónu, ktorá je normálne 100 – 1 000-krát nižšia než sekrécia kortizolu – sa reguluje hlavne angiotenzínom II a hladinou kália, pričom aj ACTH má krátkodobý účinok. Angiotenzín II stimuluje biosyntézu aldosterónu cestou aktivácie fosfatidylinozitolovej kaskády a kálium zasa depolarizuje bunkovú membránu, čím zvyšuje vstup kalcia do buniek. Tieto mechanizmy napokon aktivujú aldosterónsyntázu (CYP11B2), ktorá je potrebná pre syntézu aldosterónu. Aldosterón podporuje reabsorpciu sodíka a vylučovanie draslíka obličkami tubulárnych epitelových buniek a v distálnych tubuloch. Sodík sa vstrebáva, voda nasleduje pasívne, čo vedie k zvýšeniu objemu extracelulárnej tekutiny s malou zmenou koncentrácie plazmatického sodíka. Trvalo zvýšené objemy extracelulárnej tekutiny spôsobujú vysoký krvný tlak. To pomáha minimalizovať ďalšie zvýšenie objemu extracelulárnej tekutiny tým, že spôsobí tlakovú diurézu v obličkách. Bez aldosterónu obličky strácajú nadmerné množstvo sodíka a následne aj vodu, čo vedie k závažnej dehydratácii. Sodík sa aktívne vstrebáva, draslík sa vylučuje. Nerovnováha aldosterónu vedie pri zvýšených hladinách k hypokaliémii a k hyperkaliémii s kardiálnou toxicitou, ak sú hladiny znížené. Okrem toho dochádza k výmene sodíka a draslíka v renálnych tubuloch, vodík je v oveľa menšej miere a prebytkom aldosterónu sa môže vyvinúť mierna metabolická alkalóza. Okrem účinkov aldosterónu v renálnych tubuloch sú podobné účinky na potné a slinné žľazy. Aldosterón stimuluje reabsorpciu chloridu sodného a vylučovanie draslíka, čo pomáha zabrániť nadmernému slineniu a zachovaniu soli v horúcom podnebí. Aldosterón tiež ovplyvňuje absorpciu sodíka v čreve, najmä v hrubom. Nedostatok môže spôsobiť vodnatú hnačku z neabsorbovaného sodíka a vody. Ako som už spomínal, sekréciu aldosterónu najviac ovplyvňuje zapojenie renín-angiotenzín systému a zmeny v koncentrácii plazmatického draslíka. Renín je enzým, ktorý aktivuje angiotenzinogén a vzniká angiotenzín I. V pľúcach pomocou ACE premieňa angiotenzín I (dekapeptid) na angiotenzín II (oktapeptid), ktorý má silné vazokonstrikčné účinky a je stimulátorom uvoľňovania aldosterónu v nadobličkách.
Kortizol
Je hlavným glukokortikoidom, ktorý sa tvorí predovšetkým v zona fasciculata a k jeho tvorbe čiastočne prispieva aj zona reticularis. Približne 95 % aktivity glukokortikoidov pochádza z kortizolu a z kortikosterónu. Priebeh biosyntézy kortizolu začína v mitochondriách konverziou cholesterolu na pregnenolón. Uvoľnenie kortizolu je takmer úplne riadené sekréciou adrenokortikotropínu (ACTH) v hypofýze, ktorý je riadený kortikotropín uvoľňujúcim hormónom (CRH) – je vylučovaný z hypotalamu. V normálnych situáciách je pri CRH, ACTH a kortizole preukázaný cirkadiánny rytmus s vrcholom v skorých ranných hodinách a poklesom vo večerných hodinách. Negatívna spätná väzba účinkov kortizolu na predný lalok hypofýzy a hypotalamu pomáha toto zvýšenie kontrolovať a reguluje plazmatické koncentrácie kortizolu. Kortizol stimuluje glukoneogenézu v pečeni tým, že stimuluje zúčastnené enzýmy a mobilizuje potrebné substráty, najmä aminokyseliny zo svalov a voľných mastných kyselín z tukového tkaniva. Súčasne znižuje využitie glukózy extrahepatálnymi bunkami v tele. Výsledkom je zvýšenie glykémie (napr. nadobličkový diabetes) a zvýšené zásoby glykogénu v pečeni. Kortizol znižuje proteíny v tele (s výnimkou pečene) inhibíciou syntézy proteínov a stimuluje katabolizmus svalových bielkovín. Kortizol má klinicky významné protizápalové účinky, blokuje skorú fázu zápalu tým, že stabilizuje lyzozomálne membrány, zabraňuje nadmernému uvoľňovaniu proteolytických enzýmov, znižuje priepustnosť kapilár a v dôsledku toho sa znižuje edém a následne aj chemotaxia leukocytov. Okrem toho, že indukuje rýchle riešenie zápalu, ktorý už prebieha, je nepriaznivo ovplyvnená imunita.
Androgény
Nadobličkové pohlavné hormóny sa tvoria predovšetkým v zona reticularis, hoci ich prekurzory môže tvoriť aj zona fasciculata. Kľúčovým enzýmom pri ich produkcii je CYP17 a kľúčovým prekurzorom je dehydroepiandrosterón (DHEA), ktorý síce nemá androgénovú aktivitu, ale môže sa konvertovať na najsilnejší androgén – testosterón. U mužov je androgénová produkcia nadobličky (cca 100 ug denne) zanedbateľná v porovnaní s testes (7 000 ug denne). U žien však nadoblička produkuje okolo 50 % androgénov. Estrogény u žien aj u mužov sa tvoria v kôre nadobličky, kde vznikajú konverziou z androgénov pomocou aromatázy (estradiol z testosterónu a estrón z androstendiónu). Aromatáza sa nachádza okrem nadobličiek aj v iných tkanivách, najmä v tukovom. U normálnych žien s intaktnými ováriami je nadobličková produkcia estrogénov bezvýznamná, avšak u menopauzálnych alebo ovariektomovaných žien sa nadoblička stáva hlavným a jediným zdrojom endogénnych estrogénov. Regulácia sekrécie kortizolu je hypotalamo-hypofýzovým systémom. Hlavným hypotalamovým faktorom, ktorý stimuluje produkciu adrenokortikotropínu, je CRH. Kortizol je primárnym regulátorom pokojovej aktivity hypotalamo-hypofýzo-adrenálnej osi, a to svojím negatívnym spätnoväzbovým účinkom na vyplavenie CRH a ACTH. Môže však inhibovať aj zvýšenú sekréciu CRH. Tento negatívny účinok kortizolu nastáva na úrovni hypotalamu aj hypofýzy. Kôra nadobličiek neustále vylučuje niekoľko mužských pohlavných hormónov vrátane DHEA, DHEAS, androstendiónu a 11-hydroxyandrostendiónu, s malým množstvom ženských pohlavných hormónov (estrogénu a progesterónu). Všetky majú slabý účinok, ale pravdepodobne hrajú úlohu v ranom vývoji mužských pohlavných orgánov a majú dôležitú úlohu u žien počas puberty. ACTH má určitý stimulačný účinok na uvoľňovanie androgénov nadobličiek. (Kreze, 2004)
Diferenciálna diagnostika ochorení nadobličiek je rozsiahla a prejavuje sa nasledovne:
non-neoplastické nádory,
krvácanie,
cysta,
absces,
chronické granulomatózne ochorenie (napr. tuberkulóza, histoplazmóza),
nádorové ochorenia,
myelolipóm,
ganglioneuróm,
adrenokortikálny adenóm,
hemangióm,
feochromocytóm,
leiomyóm,
neuroblastóm,
adrenokortikálny karcinóm,
non-Hodgkin lymfóm,
leiomyosarkóm,
metastázy (napr. malígny melanóm, karcinóm prsníka, hepatocelulárny karcinóm, karcinóm pľúc dlaždicového typu).
Diferenciálna diagnostika bilaterálne zväčšených nadobličiek:
Cushingov syndróm,
nadobličková nodulárna hyperplázia,
mimomaternicové ACTH alebo kortikotropín uvoľňujúci hormón (CRH),
metastázy,
feochromocytóm,
lymfóm,
krvácanie.
Hyperkortizolizmus (Cushingov syndróm)
Komplex príznakov v dôsledku nadprodukcie kortizolu, ktorý je spôsobený primárnym ochorením nadobličiek (adenóm, hyperplázia, karcinóm), t. j. Cushingovým syndrómom v užšom zmysle slova, nadprodukciou ACTH pri adenóme alebo hyperplázii kortikotrofov hypofýzy, prípadne nadprodukciou ACTH pri iných nádoroch (paraneoplastický hyperkortizolizmus). Toto ochorenie má veľmi pestrú paletu príznakov a jedným z nich je aj artériová hypertenzia. Prevalencia hypertenzie je vysoká a závisí aj od príčiny hyperkortizolizmu – pri periférnom a centrálnom hyperkortizolizme sa pohybuje okolo 80 %, pri ektopickom až do 95 %. Pri iatrogénnom hyperkortizolizme – t. j. hyperkortizolizme navodenom liečbou glukokortikoidmi – je výskyt hypertenzie do 20 %. Diagnostika Cushingovho syndrómu patrí do kompetencie endokrinológa a vzhľadom na jeho typický klinický obraz a pestrú škálu príznakov nie je ťažká. Náročnejšia je však diagnostika tzv. subklinického Cushingovho syndrómu, pri ktorom chýbajú typické prejavy, avšak pacienti majú často príznaky metabolického syndrómu. V patogenéze hypertenzie pri Cushingovom syndróme sa uplatňuje viacero mechanizmov, napr. mineralokortikoidný efekt kortizolu, inhibičný účinok glukokortikoidov na vazodilatáciu navodenú vazodilatátormi, zvýšená aktivita renín-angiotenzínového systému, zvýšená periférna cievna rezistencia, ako aj častý výskyt obštrukčného spánkového apnoe pri tomto ochorení. V prípade aktivity ochorenia sa za najúčinnejšie antihypertenzíva považujú inhibítory ACE, sartany a blokátory kalciových kanálov, prípadne ich kombinácia. (Kreze, 2004, Lazúrová, 2013)

Primárny hyperaldosteronizmus (Connov syndróm)
Primárny hyperaldosteronizmus (PH) je definovaný ako nadmerná a relatívne autonómna produkcia aldosterónu vymykajúca sa z regulácie renín-angiotenzínového systému, ktorý je suprimovaný. U väčšiny chorých je prítomná hypokáliémia. Prevalencia primárneho hyperaldosteronizmu sa zavedením skríningu pomocou aldosterónovo-renínového pomeru výrazne zvýšila a v súčasnosti sa PH považuje za najčastejšiu príčinu endokrinnej a taktiež aj liečitelnej hypertenzie. Chorí s rezistentnou hypertenziou majú prevalenciu PH až do 20 %, t. j. každý piaty pacient s rezistentnou hypertenziou môže mať Connov syndróm. Vzhľadom na vysoký výskyt tejto hypertenzie a možnosť jej liečenia je teda dôležité ochorenie včas rozpoznať a adekvátne ho liečiť. Diagnostika a liečba Connovho syndrómu patria do kompetencie endokrinológa a internistu. Skríning by sa mal robiť u hypertonikov s hypokáliémiou, u pacientov s incidentalómami nadobličiek, u pacientov so závažnou hypertenziou, rezistentnou hypertenziou a u hypertonikov v mladom veku. Riziko kardiovaskulárnych a cievnych mozgových príhod je u pacientov s PH vyššie než u chorých s primárnou hypertenziou. Skríning primárneho hyperaldosteronizmu sa odporúča realizovať stanovením pomeru aldosterón/renín a pri jeho zvýšených hodnotách (> 400, ak je aldosterón udávaný v pg/ml a renín v ng/ml) je potrebné vykonať potvrdzujúce testy. Pri testovaní pacienta musíme zachovať určité podmienky, t. j. musíme upraviť hladinu kaliémie nad 3,0 mmol/l, pacient má normálny prívod soli, estrogény a spironolaktón musí vynechať 6 týždňov pred vyšetrením. Z ostatných antihypertenzív možno použiť pred vyšetrením len tie, ktoré neovplyvňujú aldosterónovo-renínový pomer (kalciové blokátory a alfa-blokátory). Beta-blokátory výrazne zvyšujú ARR, preto je potrebné vynechať ich pred testovaním aspoň na týždeň. Jedinou úspešnou liečbou PH je adrenalektómia, ak je PH spôsobený adenómom produkujúcim aldosterón. Pri tzv. idiopatickom hyperaldosteronizme, ktorého morfologickým podkladom je unilaterálna alebo bilaterálna hyperplázia nadobličiek, je indikovaná medikamentózna liečba. Používajú sa blokátory aldosterónových receptorov.
Z ostatných antihypertenzív sú účinné blokátory kalciového kanála, ACE inhibítory a sartany. Po úspešnej operácii aldosterón-produkujúceho adenómu je regresia hypertenzie asi v 50 – 70 % prípadoch. (Lazúrová, 2013)
Addisonova choroba
Ide o pomerne vzácne, ale veľmi vážne endokrinné ochorenie. Jeho podstata je v zlyhaní nadobličiek v produkcii hormónov kortizolu a aldosterónu. Kortizol, ktorý patrí medzi glukokortikoidy, má vplyv na metabolizmus a imunitu organizmu a to predovšetkým v stresových situáciách. Aldosterón zaraďujeme do skupiny mineralokortikoidov a jeho hlavná funkcia spočíva v hospodárení s iónmi a udržiavaní správnych hodnôt krvného tlaku. Choroba môže byť primárna – keď je na vine porucha nadobličiek – alebo sekundárna – keď sa problém skrýva v hypotalame, kde je regulovaná aktivita nadobličiek. Podľa príčin delíme Addisonovu chorobu na dve formy: centrálnu a periférnu. Centrálna forma je menej častá. Je spôsobená poškodením hypotalamu, najčastejšie nádormi, infekciami a poranením. Nadobličky sú v poriadku, ale chýba im riadiaci hormón, ktorý je produkovaný práve hypotalamom. Periférna forma je podmienená poruchou kôry nadobličiek. Príčinou býva postihnutie tkaniva nadobličiek zápalom, metastázami či autoimunitným ochorením. Sekundárne sa táto forma ochorenia môže pridať k iným chorobám, ako je napríklad AIDS alebo tuberkulóza. Na nedostatok hormónov reaguje organizmus celkovou únavou, podráždenosťou, stratou na váhe a nechutenstvom. Chorý má zároveň chuť na veľmi slané potraviny. Nedostatok aldosterónu vedie k nahromadeniu draslíka v organizme, čo spôsobí hnačky, ale aj smrteľne nebezpečné poruchy srdcového rytmu. Navonok sa choroba prejavuje hyperpigmentáciou kože, chorý tak paradoxne vyzerá zdravo opálený. Na živote ohrozujúca je predovšetkým iónová dysbalancia a zlá regulácia krvného tlaku, ktorý je veľmi nízky. K diagnóze často dovedú už samotné príznaky a vyšetrenie krvi – predovšetkým hodnoty iónov a hormónov. Stav obličiek je kontrolovaný pomocou ultrazvuku, poruchy hypotalamu rozpoznáme pomocou CT a magnetickej rezonancie. Príznaky tohto ochorenia sa objavujú postupne a súvisia hlavne s nedostatkom kortizolu (glukokortikoidy) a aldosterónu (mineralokortikoidy). Nedostatok androgénov sa zväčša prejavuje len minimálne.
Príznaky a znaky tohto ochorenia sú:
vznik postupnej svalovej slabosti s nadmernou únavnosťou stupňujúcou sa v priebehu dňa, spolu s nechutenstvom a stratou telesnej hmotnosti,
zjavenie sa hnedých pigmentových škvŕn na odhalených častiach kože, ako sú tvár a dlane, ďalej v oblasti genitálu, análneho otvoru a prsných dvorcov; škvrny (alebo tmavšie sfarbenie) sa vyskytujú aj na sliznici ústnej dutiny,
pokles krvného tlaku následkom straty cirkulujúcej vody,
napínanie na zvracanie, zvracanie, bolesti brucha, znížená tvorba žalúdočnej kyseliny, hnačky,
strata ochlpenia následkom zníženej tvorby androgénov,
nervozita, podráždenosť, spontánne sťahy svalstva, poruchy pamäti a s tým súvisiace narušenie intelektových funkcií, čo môže vyústiť do stavov zmätenosti a ťažkej depresie.
Diagnostika Addisonovej choroby sa zakladá na stanovení hladín kortikoidov v krvi po stimulácii nadobličiek určitými testami. Táto skupina testov slúži na potvrdenie diagnózy pri podozrení na ochorenie na podklade vyššie vymenovaných príznakov a znakov. Liečba spočíva v umelom dodávaní chýbajúcich hormónov po zvyšok pacientovho života. Prognóza tohto ochorenia je pri včasnej diagnostike veľmi dobrá. Ak pacient následne spolupracuje pri liečbe, je očakávaná dĺžka života prakticky rovnaká ako pri ostatnom obyvateľstve. (Lazúrová 2013, Podoba, Trejbalová, Štekláč, 2005)
Feochromocytóm
Feochromocytóm je tumor, ktorý produkuje zvýšené množstvo katecholamínov. Ak nie je včas diagnostikovaný a liečený, končí fatálne – často ako infarkt myokardu alebo mozgová príhoda. Z 90 % sa nachádza v chromafinnom tkanive drene NO a z 10 % je extraadrenálne uložený v sympatickom nervstve a nazýva sa paraganglióm. Často je súčasťou syndrómu MEN2A. Feochromocytóm je „herec“ a okrem vysokého tlaku krvi nemusia mať pacienti žiadne iné príznaky, avšak pri náhlom vyplavení hormónov sa u nich môže vyskytnúť prudká bolesť hlavy, zrýchlený pulz, potenie a vtedy je pacient ohrozený aj vznikom závažnej poruchy srdcového rytmu alebo mozgovou príhodou, prípadne infarktom myokardu. Mali sme viacerých pacientov, u ktorých feochromocytóm spôsobil infarkt myokardu. Zriedkavejšie sa môžu vyskytnúť zvýšené teploty, chudnutie, zápcha a nevysvetliteľné potenie. Liečba nádoru je výlučne chirurgická, avšak dôležitá je príprava pred operáciou, ktorá si vyžaduje špecifickú liečbu vysokého tlaku. Bez tejto liečby by bol operačný výkon veľmi rizikový. Pri liečbe je nevyhnutná úzka spolupráca internistu-endokrinológa, anesteziológa a chirurga, pričom všetci by mali mať skúsenosti s diagnostikou a liečbou tohto ochorenia. Väčšina feochromocytómov sa vyskytuje sporadicky, ale až v 30 % prípadov sa môžu vyskytovať familiárne. Familiárne feochromocytómy sú často multifokálne a bilaterálne. Feochromocytómy sa vyskytujú asi u 0,1 % pacientov s rôznym stupňom artériovej hypertenzie (5 na milión obyvateľov). Na Slovensku by teda mohlo byť odhadom cca 25 nových ochorení ročne. Asi 50 % chorých má fixovanú hypertenziu a ďalších 50 % má hypertenziu paroxyzmálnu a medzi paroxyzmami sú pacienti normotenzní. Menej často sa feochromocytóm prezentuje hypotenziou, najmä posturálnou – to je hlavne v prípadoch secernujúcich adrenalín alebo látky spôsobujúce vazodilatáciu. Najčastejším prejavom (v 90 %) je však artériová hypertenzia. Diagnostika feochromocytómu sa opiera o laboratórny dôkaz nadprodukcie katecholamínov a ich metabolitov. S prihliadnutím na senzitivitu sa v súčasnosti ako základné testovanie odporúča vyšetrenie voľných plazmatických nefrínov s 99-percentnou senzitivitou. Na skríning sú vhodné aj močové katecholamíny, majú však nižšiu senzitivitu. V prípade normálnych hodnôt je feochromocytóm vysoko nepravdepodobný. V prípade hodnôt normetanefrínu nad 1 nmol/l a metanefrínu nad 0,5 nmol/l je tumor vysoko pravdepodobný a nasledujú lokalizačné metódy. Ak sú však hodnoty nefrínov 4 x URL (horná hranica referenčného rozpätia), feochromocytóm je takmer na 100 % potvrdený. (Blažíček, Pacák 2004, Pacák, Goldstein a spol., 2001) Na zobrazenie feochromocytómu sa používajú zobrazovacie metódy, hlavne I123MIBG, F18-DA, F18-DOPA, CT a MRI. USG zobrazí feochromocytóm ojedinele. Po lokalizácii je jedinou úspešnou liečbou feochromocytómu chirurgické odstránenie tumoru. Pokiaľ sa nádor neodstráni, symptómy sa môžu zhoršovať s rastom tumoru a zvýšený krvný tlak zapríčinený týmto nádorom môže poškodiť ďalšie orgány, predovšetkým srdce a obličky, pričom u pacienta sa zvyšuje riziko srdcového alebo mozgového infarktu. Asi 20 % pacientov má aj naďalej hypertenziu, ktorá je však omnoho ľahšie kontrolovaná antihypertenzívnou liečbou. Typické príznaky feochromocytómu sú záchvaty vysokého krvného tlaku – hypertenzie, bolesti hlavy, potenie, búšenie srdca, zvýšená pulzová frekvencia, zväčšené srdce, náhle zblednutie tváre, zriedkavo sčervenanie tváre, hrudníka, psychické poruchy, porucha regulácie metabolizmu glukózy, chudnutie. (Blažíček, Lángoš, 2012). Na feochromocytóm treba myslieť u pacienta s AH rezistentnou na štandardnú liečbu. Hypertenzia dobre odpovedá na alfa-blokátory (napr. prazosín), blokátory kalciového kanála (najmä amlodipín) alebo nitroprusid. Zhoršuje sa po beta-blokátoroch, ktoré sú kontraindikované ako monoterapia AH pri feochromocytóme. Možno ich podávať iba súčasne s alfa-blokátorom, pričom je výhodné, ak kombinovanej liečbe predchádza terapia alfa-blokátorom. (Podoba, Trejbalová, Štekláč, 2005)

Záver
Biochemická diagnostika je napriek výraznému pokroku zobrazovacích metód v diferenciálnej diagnostike veľmi dôležitá. Počas anamnestického vyšetrovania pacienta sa lekár stretáva s veľkým počtom symptómov príznačných pre mnohé ochorenia. Žiadny z tumorov alebo ochorení nevytvára väčšiu pestrosť klinického obrazu než feochromocytóm. Práve variabilita symptómov by mala u ošetrujúceho lekára vzbudiť podozrenie na feochromocytóm, najmä pri hypertenzii a pri predoperačnom vyšetrení. Jediným spoľahlivým diferenciálne diagnostickým príznakom feochromocytómu je stanovenie metabolitov katecholamínov v moči a krvi. Tie majú byť stanovené pred rozhodnutím o operačnej liečbe, lebo súčasné biochemické metódy umožňujú diagnózu feochromocytómu približujúcu sa 100 % a operačné riziko v rukách erudovaného tímu pri poznanom feochromocytóme pred operáciou klesá voči nerozpoznanému tumoru na zlomky percenta. Je dôležité pristupovať k anamnéze pacienta s podozrením a pýtať sa na cenné príznaky, ktoré pacienta sprevádzajú. Pacienti totiž niektoré príznaky spontánne nekomentujú, lebo môžu byť mierne, takže si ich nevšímajú, alebo ich nesprávne interpretujú – najmä ak je príznakov málo, alebo chýbajú. Subjektívne ťažkosti – ako aj objektívne príznaky – môžu byť veľmi rôznorodé a môžu simulovať početné syndrómy.
Literatúra
- Kreze A., Langer P., Klimeš I., Stárka L., Payer J., Michálek J.: Všeobecná a klinická endokrinológia s. 351 – 412, AEP, 2004
- Blažíček P., Lángoš J.: Mnohopočetná endokrinná neoplázia, 2012
- Blažíček P.: Biochemická diagnostika feochromocytómu. Interná medicína s. 10 – 15, 2011
- Blažíček P., Pacák K.: Nekonjugované metanefríny v plazme: význam a možnosti stanovenia. Interná med, 4, 2004;9 (S3): 38
- Lazúrová I.: Problém endokrinnej hypertenzie, Lekárske listy, uverejnené 17. 1. 2013
- Pacák K., Goldstein DS a spol.: A „pheo“ lurks: novel approoaches for lokating occult pheochromocytoma J. Clin. Endocrinol Metab. 86:3641 – 3646, 2001
- Podoba J., Trejbalová L., Štekláč J.: Úloha praktického lekára v diagnostike hormonálne podmienenej sekundárnej artériovej hypertenzie Via pract., 2005, roč. 2 (5): 243 – 247